O equilíbrio químico ocorre quando, em uma reação reversível, a velocidade da reação direta é igual à velocidade da reação inversa. Nesse momento, as concentrações de reagentes e produtos permanecem constantes ao longo do tempo, embora a reação continue acontecendo em nível microscópico. É importante lembrar: equilíbrio químico não significa que a reação parou, mas sim que ela atingiu um equilíbrio dinâmico.
Reações Reversíveis
São representadas por uma seta dupla: A+B⇌C+D
Um exemplo clássico é o processo de produção de amônia no Processo Haber-Bosch: N2(g)+3H2(g)⇌2NH3(g)
- Nitrogênio e hidrogênio formam amônia (reação direta)
- Amônia pode se decompor novamente em nitrogênio e hidrogênio (reação inversa)
Constante de Equilíbrio (Kc)
A constante de equilíbrio expressa a relação entre as concentrações de produtos e reagentes:
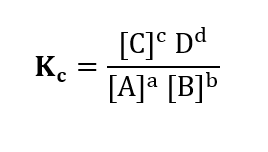
Onde:
- As letras minúsculas representam os coeficientes da equação balanceada.
- Colchetes indicam concentração molar (mol/L).
Interpretação de Kc
- Kc > 1 → equilíbrio favorece os produtos
- Kc < 1 → equilíbrio favorece os reagentes
- Kc ≈ 1 → quantidades semelhantes de reagentes e produtos
Fatores que Influenciam o Equilíbrio
(Princípio de Le Châtelier)
O químico francês Henri Le Châtelier afirmou que:
Quando um sistema em equilíbrio sofre uma perturbação, ele tende a se ajustar para minimizar essa perturbação.
1️⃣ Concentração
- Aumentar reagentes → desloca para a direita
- Aumentar produtos → desloca para a esquerda
2️⃣ Temperatura
- Reação endotérmica: ↑T favorece produtos
- Reação exotérmica: ↑T favorece reagentes
3️⃣ Pressão (em reações com gases)
- ↑Pressão → favorece o lado com menor número de mols gasosos
Equilíbrio Homogêneo e Heterogêneo
- Homogêneo: todas as substâncias na mesma fase (ex: todos gases).
- Heterogêneo: substâncias em fases diferentes (sólido + gás, por exemplo).
Exemplo heterogêneo: CaCO3(s)⇌CaO(s)+CO2(g)
(Sólidos não entram na expressão de Kc.)
Aplicações do Equilíbrio Químico
- Produção industrial de fertilizantes
- Controle do pH no sangue
- Processos biológicos
- Indústria farmacêutica
- Tratamento de água

0 comentário