A distribuição eletrônica é a forma como os elétrons estão organizados ao redor do núcleo de um átomo. Compreender essa organização é fundamental para entender as propriedades químicas dos elementos, como reatividade, formação de ligações químicas e comportamento periódico. Um dos métodos mais utilizados para realizar a distribuição eletrônica é o Diagrama de Linus Pauling, desenvolvido com base nos estudos do químico norte-americano Linus Pauling, vencedor de dois Prêmios Nobel (Química e Paz).

O que é Distribuição Eletrônica?
A distribuição eletrônica descreve como os elétrons se organizam em:
- Níveis de energia (camadas) – Representados por números (1, 2, 3, 4, 5, 6 e 7) ou pelas letras K, L, M, N, O, P e Q.
- Subníveis de energia – Representados pelas letras: s, p, d, f
Digamos que os subníveis são as subcamadas e cada subnível comporta uma quantidade máxima de elétrons:
| Subnível | Nº máximo de elétrons |
| s | 2 |
| p | 6 |
| d | 10 |
| f | 14 |
O Diagrama de Linus Pauling
O Diagrama de Linus Pauling organiza os subníveis em ordem crescente de energia. Ele é representado por linhas diagonais que indicam a sequência correta de preenchimento dos orbitais.
A ordem de preenchimento é:
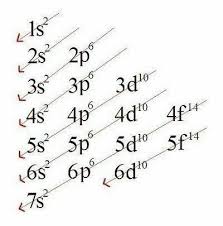
Seguindo as diagonais, temos a sequência:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p
Essa ordem não segue exatamente a sequência numérica simples (1, 2, 3…), pois considera a energia relativa dos subníveis.
Como Fazer a Distribuição Eletrônica?
Para realizar a distribuição eletrônica de um elemento:
- Descubra o número atômico (Z).
- Esse número corresponde à quantidade de elétrons no átomo neutro.
- Preencha os subníveis seguindo a ordem do diagrama de Pauling.
- Respeite o limite máximo de elétrons por subnível.
Exemplo: Oxigênio (Z = 8)
Distribuindo 8 elétrons:
1s² 2s² 2p⁴
Exemplo: Ferro (Z = 26)
1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶
Regras Importantes
Além do Diagrama de Pauling, três princípios orientam a distribuição eletrônica:
- Princípio da Energia Mínima (Aufbau): os elétrons ocupam primeiro os subníveis de menor energia.
- Princípio da Exclusão de Pauli: um orbital comporta no máximo dois elétrons com spins opostos.
- Regra de Hund: em subníveis do tipo p, d e f, os elétrons ocupam primeiro orbitais vazios antes de formar pares.
Importância da Distribuição Eletrônica
A distribuição eletrônica permite:
- Entender a organização da Tabela Periódica;
- Identificar elétrons da camada de valência;
- Prever formação de ligações químicas;
- Compreender propriedades como raio atômico e eletronegatividade.
Conclusão
O Diagrama de Linus Pauling é uma ferramenta essencial no estudo da Química. Ele organiza os subníveis em ordem energética e facilita a compreensão da estrutura eletrônica dos átomos. Ao dominar esse conteúdo, o estudante passa a entender melhor o comportamento químico dos elementos e suas interações.
0 comentário